myc驅(qū)動的肝臟腫瘤發(fā)生機制尚不清楚。該研究表明,在肝細(xì)胞特異性Ptpn11/ Shp2缺失的小鼠中,Mycdriven肝癌(HCC)顯著加重。然而,在Shp2缺失的肝臟中,Myc誘導(dǎo)的腫瘤選擇性地從罕見的Shp2陽性肝細(xì)胞中發(fā)展,Myc驅(qū)動的腫瘤發(fā)生依賴于由Shp2促進的完整Ras-Erk信號傳導(dǎo)來維持Myc的穩(wěn)定性。盡管對Shp2細(xì)胞自主生長有嚴(yán)格的要求,但Shp2的缺失會導(dǎo)致免疫抑制環(huán)境,導(dǎo)致腫瘤起始細(xì)胞的清除缺陷和腫瘤的侵襲性進展。
基礎(chǔ)Wnt/b-catenin信號通路在shp2缺失的肝臟中上調(diào),Myc轉(zhuǎn)染進一步增強了這一信號通路。消融Ctnnb1抑制myc誘導(dǎo)的shp2缺陷肝細(xì)胞癌,揭示了b-catenin的重要作用。Myc過表達和CTNNB1突變在預(yù)后不良的HCC患者中經(jīng)常同時檢測到。這些數(shù)據(jù)闡明了肝臟腫瘤發(fā)生的復(fù)雜機制,其驅(qū)動因素是細(xì)胞固有的致癌信號,以及通過干擾特定的致癌途徑產(chǎn)生的促腫瘤微環(huán)境。

圖片來源:https://doi.org/10.1016/j.celrep.2021.1099
原發(fā)性肝癌是一種高致死率的疾病,在世界范圍內(nèi)發(fā)病率和死亡率均呈上升趨勢。肝臟腫瘤的發(fā)生是由一系列的增殖、代謝和結(jié)構(gòu)改變引起的慢性肝臟疾病。HCC的特點是化療耐藥,通常在晚期診斷,治療選擇有限。盡管治療效果不佳,但多激酶抑制劑索拉非尼十年來一直是治療晚期HCC的一線藥物。
美國食品和藥物管理局(FDA)最近才批準(zhǔn)atezolizumab和bevacizumab的聯(lián)合治療,在不可切除的HCC中,其總體生存率和腫瘤無進展生存率明顯優(yōu)于索拉非尼。未來開發(fā)更有效的基于機制的治療方法需要更深入地了解肝臟中相互交織的細(xì)胞內(nèi)在和細(xì)胞外致瘤信號。
Shp2/Ptpn11是一種含有sh2的酪氨酸磷酸酶,作用于受體酪氨酸激酶(RTKs)和細(xì)胞因子受體的下游。遺傳和生化分析顯示,Shp2在介導(dǎo)rtk激活Ras/Erk通路中發(fā)揮了積極作用。雖然其促進Erk信號轉(zhuǎn)導(dǎo)的生物學(xué)意義尚不完全清楚,但Shp2確實是第一個被發(fā)現(xiàn)的致癌酪氨酸磷酸酶,在白血病和實體腫瘤中檢測到Ptpn11的顯性活性突變。
藥物抑制Shp2可以有效抑制由rtk引發(fā)的致癌信號驅(qū)動的癌細(xì)胞的增殖。在肝細(xì)胞中刪除Shp2可以抑制HGF受體MET與其他腫瘤蛋白聯(lián)合驅(qū)動的肝腫瘤發(fā)生。然而,Shp2缺乏也加重了化學(xué)致癌物二乙亞硝胺(DEN)誘導(dǎo)的HCC,并加速了pten缺陷肝臟中非酒精性脂肪性肝炎(NASH)驅(qū)動的肝臟腫瘤發(fā)生。總的來說,這些研究揭示了Shp2在肝臟中自相矛盾的抗腫瘤和促腫瘤作用,其潛在機制尚不清楚。
c-Myc (Myc)的異常表達與所有人類癌癥的50%有關(guān),也與動物模型中各種實驗性誘導(dǎo)腫瘤有關(guān)。特別是Myc過表達在預(yù)后不良的侵襲性肝癌和肝母細(xì)胞瘤中。然而,在轉(zhuǎn)基因小鼠中,Myc單獨驅(qū)動HCC發(fā)展效率低下,但需要另一種致癌基因的共同表達或同時刪除一種抑癌基因。基因組分析顯示,在肝癌患者和小鼠HCC模型中,Myc擴增和CTNNB1/ b-catenin突變經(jīng)常同時發(fā)生。b-Catenin與Myc啟動子結(jié)合并驅(qū)動Myc表達。
通過上位分析,Myc 明顯位于腸道中 APC/b-catenin 的下游,但 Myc 缺失并不能抑制肝臟中 APC 丟失的影響,盡管去除 b-catenin 確實有效。Wnt/b-catenin信號通路控制的肝臟氨代謝酶的分區(qū)也發(fā)現(xiàn)與Myc無關(guān)。因此,Myc和b-catenin在肝臟特異性環(huán)境下協(xié)同致瘤作用的機制尚不完全清楚。
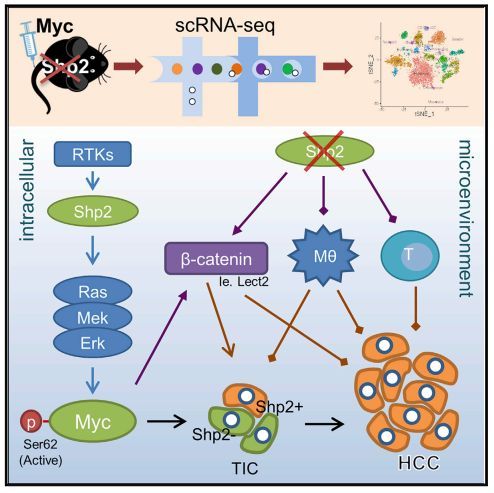
單細(xì)胞轉(zhuǎn)錄組學(xué)揭示了Shp2在myc驅(qū)動的肝腫瘤細(xì)胞和微環(huán)境中的相反作用
圖片來源:https://doi.org/10.1016/j.celrep.2021.109974
本研究結(jié)合單細(xì)胞rna測序(scRNA-seq)與功能和分子分析,揭示了Shp2在肝臟腫瘤發(fā)生中的雙向功能的復(fù)雜機制。值得注意的是,作者發(fā)現(xiàn)在Myc驅(qū)動的HCC中,通過保持Myc上游完整的Ras/Erk通路,Shp2是細(xì)胞自主需要的。同時,Shp2缺失也在肝臟中誘導(dǎo)了促進腫瘤的微環(huán)境。
綜上所述,這些結(jié)果闡明了一種新的腫瘤細(xì)胞內(nèi)在和外在因素交織驅(qū)動最嚴(yán)重的腫瘤表型的嵌合機制。本研究闡明了之前記錄的Shp2酪氨酸磷酸酶在癌癥中的相互矛盾的作用,這將有助于設(shè)計更有效的惡性疾病治療方法。




 17312606166
17312606166