近日,上海交通大學章雪晴教授、新澤西理工學院許曉陽教授團隊合作,在 Nature Communications 期刊發表了題為:mRNA lipid nanoparticle-mediated pyroptosis sensitizes immunologically cold tumors to checkpoint immunotherapy 的研究論文。
該研究提出了一種基于mRNA的細胞焦亡納米藥物治療方法,它能夠啟動癌癥免疫周期,將冷腫瘤轉化為炎癥細胞因子表達和T細胞浸潤的熱腫瘤,從而有效治療免疫冷腫瘤。

細胞焦亡(pyroptosis)是一種炎癥性程序性細胞死亡,由gasdermin(GSDM)家族蛋白的蛋白水解性裂解觸發。GSDM通常通過其N端和C端結構域的分子內相互作用而自我抑制。在連接區被特異性半胱氨酸天冬氨酸蛋白酶和其他蛋白酶裂解后,壞死性端結構域形成低聚物并轉移到質膜。游離N端結構域與脂質成分結合并在細胞膜上并打孔,導致質膜快速破裂,并釋放危險相關分子模式(DAMP)和促炎細胞因子。免疫細胞識別特定的DAMP,進而觸發一系列免疫反應,包括免疫細胞的激活和浸潤。此外,通過焦亡孔釋放的促炎細胞因子有助于逆轉免疫抑制性腫瘤微環境(TME)。
盡管這些發現令人鼓舞,但許多癌癥中GSDM的低表達和復雜的裂解過程阻礙了通過遞送蛋白酶來觸發細胞焦亡以產生抗腫瘤免疫。
研究團隊推測通過直接傳遞N末端GSDM結構域誘導的細胞焦亡是在癌癥免疫周期中引發一系列事件并將冷腫瘤轉化為熱腫瘤的有效方法。
基于mRNA納米藥物的基因治療具有廣闊的臨床應用前景。最近,該成功開發了一種可合成的可電離陽離子脂質納米顆粒(AA3-Dlin LNPs)的制劑,該制劑具有良好的安全性和較高的體內外mRNA翻譯效率。mRNA-LNPs與GSDM協同激活細胞焦亡,有望在腫瘤治療中發揮重要作用。
在該研究中,我們提出了一種基于mRNA的納米醫學方法,其中AA3-Dlin LNP配方封裝了一個編碼GSDMB N-端結構域的單劑mRNA——GSMDBNT mRNA@LNP。開發的GSMDBNT mRNA@LNP配方由可電離陽離子脂質(AA3-Dlin)、磷脂、膽固醇和PEG自組裝,GSMDBNT mRNA通過靜電相互作用被包裹在LNP內。
研究團隊期望這種LNP可以被遞送到腫瘤組織中,在那里,mRNA被翻譯為GSDMB蛋白的端結構域,并直接觸發細胞焦亡,而不需要蛋白酶裂解。
細胞焦亡具有誘導免疫細胞死亡、啟動促炎細胞因子釋放以及激活和招募腫瘤內免疫細胞的能力,進而導致一系列事件,進一步促進細胞死亡、細胞因子釋放和免疫應答激活。由此產生的正反饋回路可創建有利的免疫原性熱腫瘤微環境,使癌細胞對免疫檢查點阻斷(ICB)介導的免疫治療敏感,顯示出優于單藥治療的腫瘤抑制作用。
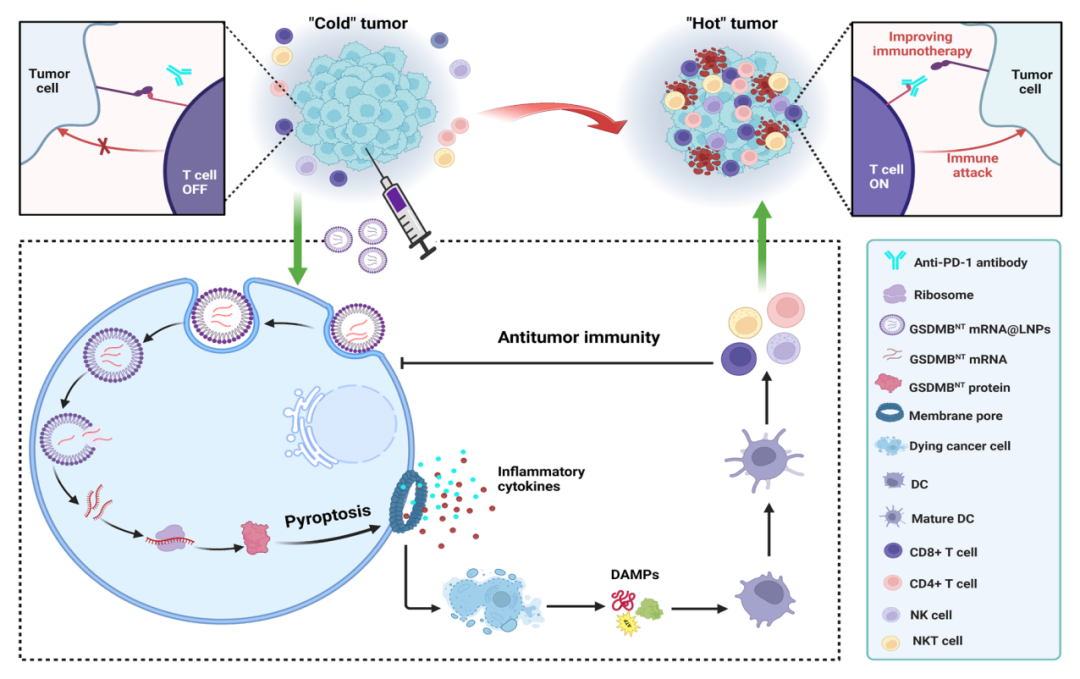
體外細胞實驗結果表明,即使由單藥GSMDBNT mRNA@LNP觸發的低水平腫瘤細胞焦亡也足以誘導穩定的免疫原性細胞死亡。
在多個免疫冷腫瘤小鼠模型中,研究結果表明,mRNA-LNP觸發的細胞焦亡可以抑制腫瘤生長和延長小鼠模型總生存期,并伴有促炎細胞因子的刺激和促進腫瘤微環境中免疫細胞的募集。
此外,mRNA-LNP觸發細胞焦亡還可以提高免疫檢查點抑制劑(aPD-1)介導的免疫治療的療效,甚至在原位4T1乳腺癌和高度侵襲性B16F10黑色素瘤模型中實現腫瘤消除和長期生存。
此外,該研究還發現,mRNA-LNP觸發細胞焦亡可以與aPD--1介導的免疫治療有效協同治療效果,誘導局部免疫應答,進而產生全身效應,根除黑色素瘤和抑制遠端腫瘤的生長。
綜上所述,該研究表明,基于mRNA的細胞焦亡納米藥物提供了一種簡單而高效的策略,以實現強大的抗腫瘤免疫和增強免疫冷腫瘤的免疫治療效果。更重要的是,該研究提供了一個通用平臺,有望擴展到免疫檢查點阻斷療法之外的其他免疫治療方法,具有很高的轉化應用前景。




 17312606166
17312606166