人的心臟在出生后幾乎完全喪失再生能力�。因此�����,心肌受損---例如心臟病發作---通常會導致成年人永久性喪失功能����。在一項新的研究中,來自德國馬克斯-普朗克心肺研究所的研究人員如今首次在小鼠身上證實心肌細胞能量代謝的改變能夠使心臟再生��。因此���,小鼠的心臟功能可以在心臟病發作后得到很大程度的恢復����。這一發現具有開創性意義,可能能夠導致全新的治療方法���。相關研究結果發表在2023年10月19日的Nature期刊上,論文標題為“Inhibition of fatty acid oxidation enables heart regeneration in adult mice”�����。

成體心臟之所以喪失再生能力��,主要是因為心肌細胞在出生后喪失了分裂能力。與此同時����,心肌細胞的能量代謝也發生了根本變化:它們不再從糖分(即糖酵解)中獲取能量����,而是主要從脂肪中獲取能量。這種能量產生方式被稱為脂肪酸氧化(fatty acid oxidation)�����。
論文共同通訊作者�����、馬克斯-普朗克心肺研究所主任Thomas Braun領導的一個研究團隊開始尋找促進心臟再生的新方法�。論文第一作者Xiang Li和論文共同通訊作者Xuejun Yuan解釋說�����,“眾所周知�,能夠使心臟再生的動物物種主要使用糖分和糖酵解作為心肌細胞的燃料�����。人類心臟在發育初期也主要使用糖酵解�����,但隨后會轉用脂肪酸氧化����,因為它能產生更多能量。隨著出生后能量產生的轉換,許多基因的活性發生了變化���,細胞分裂活性也隨之喪失。來自能量產生的代謝物對調節基因活性的酶的活性也有重要作用。因此�,我們希望通過重編程能量代謝來引發基因活性的變化��,從而重新開啟心肌細胞的細胞分裂能力。”
脂肪酸氧化基因失活
為此����,這些作者首先使小鼠體內一個名為Cpt1b的基因失活���,該基因是脂肪酸氧化所必需的���。Li解釋說�����,“我們隨后觀察到,這些小鼠的心臟開始重新生長��?!痹趯嶒炦^程中,這些小鼠心臟中的細胞數量幾乎翻了一番。下一步���,他們在關閉了Cpt1b的小鼠中引發了心臟病發作。
在這種所選擇的方法中,心臟缺血階段之后是再灌注階段,在這一階段中���,心臟會重新獲得含氧血液。Yuan解釋說,“這種模式相當于心臟病患者因冠狀動脈閉塞而插入支架來治療心臟��。效果令人印象深刻:幾周后�����,心肌中原本常見的瘢痕組織幾乎看不出來了,缺乏Cpt1b的小鼠的心臟收縮能力幾乎恢復到梗塞前的水平�����?����!?/p>
恢復再生能力
在進一步的研究中�����,這些作者成功破譯背后的內在機制。Braun解釋說�,“在基因失活的小鼠心肌細胞中���,我們發現α-酮戊二酸的水平增加了20倍�。高水平的這種代謝物導致 KDM5 酶的活性顯著增加。”
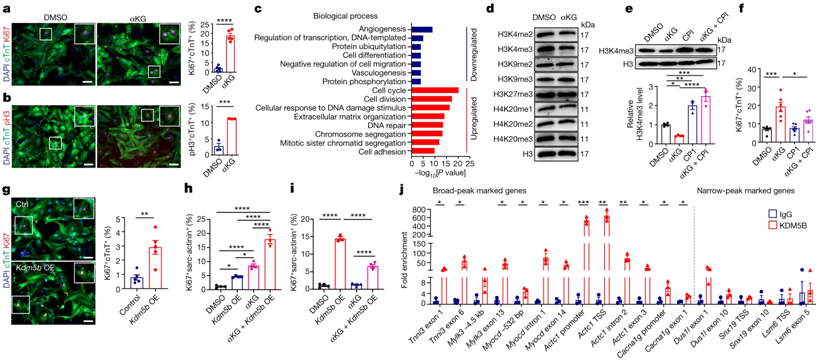
α-酮戊二酸的積累刺激了KDM5活性��,減緩了心肌細胞的成熟�����,促進了心肌細胞的增殖�。圖片來自Nature, 2023, doi:10.1038/s41586-023-06585-5�。
這種酶是一種所謂的組蛋白去甲基化酶,它能去除組蛋白中的甲基,從而降低多種基因的活性。這種基因活性的改變會使心肌細胞變得不成熟,從而恢復再生能力。
Braun認為這項新的研究是一個真正的突破�����?���!巴ㄟ^對心肌細胞代謝進行重編程���,我們將心肌細胞的數量增加了一倍�����,而且在心肌梗塞后�,心臟功能幾乎可以完全恢復�。”此外�,原則上可以通過藥物阻斷 Cpt1b 基因產物 CPT1B的酶活性����。開發一種可用于影響 CPT1B 酶活性的抑制劑����,是開發最終可用于人體的療法的下一步研究工作。
不過���,Yuan和Braun強調說,“要想在人類身上實現可靠的治療����,我們還有很長的路要走�?�;A研究新成果的實施過程漫長而昂貴���,而且往往伴隨著許多意想不到的問題���。盡管如此���,我們相信,未來我們將能夠通過治療激發心臟的再生能力��?�!?/p>




 17312606166
17312606166